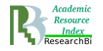Liskina Iryna Valentynovna
Doctor of Medical Science, senior researcher,
the Head of the laboratory of pathomorphology
SO «National institute of phthisiology and pulmonology named after F.G. Yanovsky National academy of medical sciences of Ukraine», Kiyv, Ukraine
Tereshkovych Aleksandr Vladymyrovych
Candidate of medical Sciences, senior scientist of
Thoracic Surgery and Invasive Diagnostic Methods Department
SO «National institute of phthisiology and pulmonology named after F.G. Yanovsky National academy of medical sciences of Ukraine», Kiyv, Ukraine
Zahaba Lyudmila Mikhailovna
Candidate of medical Sciences, researcher of
the laboratory of pathomorphology
SO «National institute of phthisiology and pulmonology named after F.G. Yanovsky National academy of medical sciences of Ukraine», Kiyv, Ukraine
Лискина Ирина Валентиновна
доктор медицинских наук, заведующая лабораторией патоморфологии
Государственного учреждения «Национальный институт фтизиатрии и пульмонологии им. Ф.Г. Яновского НАМН Украины», г. Киев, Украина
Терешкович Александр Владимирович
кандидат медицинских наук, старший научный сотрудник отделения
торакальной хирургии и инвазивных методов диагностики
Государственного учреждения «Национальный институт фтизиатрии и пульмонологии им. Ф.Г. Яновского НАМН Украины», г. Киев, Украина
Загаба Людмила Михайловна
кандидат медицинских наук, научный сотрудник
лаборатории патоморфологии
Государственного учреждения «Национальный институт фтизиатрии и пульмонологии им. Ф.Г. Яновского НАМН Украины», г. Киев, Украина
Tissue patterns of expression of CD68 + cells and antigens
M. Tuberculosis according to the results of a study of operative material in multidrug-resistant pulmonary tuberculosis
Тканевые особенности экспрессии CD68+ клеток и антигенов
M. Tuberculosis по результатам исследования операционного материала при мультирезистентном туберкулезе легких
Summary. Recently the study of the morphological features of tuberculosis caused by multidrug-resistant MBT strains remains important. The influence of morphologically different activity of inflammation at the time of surgical treatment of pulmonary MDR-TB with different clinical forms of the process on the further course of the disease, the effectiveness of surgical treatment remains poorly understood.
Refining the morphological characteristics of the tuberculous process according to the operational material is important for predicting the further development of the process, clarifying the nature of local immunity of the lungs, which can serve as a basis for clarifying and choosing the optimal further tactics of medical management of these patients.
Objective: to determine the localization and character of the expression of cells of the macrophage series, including macrophages infected with mycobacteria in the lung tissue in various forms of multidrug-resistant tuberculosis.
Material and methods. The resected fragments of the lungs from 39 patients, with the presence of tuberculoma, solitary and multiple, or suffering from pulmonary CT are investigated. In all cases microbiological examination diagnosed lung MDR-TB. Among patients were 19 men (48.7%) and 20 women (51.3%), the average age was 32.7 ± 2.3 and 38.5 ± 9.7 years, respectively. A traditional histological study of the affected lung tissue stained with hematoxylin and eosin, as well as immunohistochemistry with the use of antibodies CD68 Clon KP1 (TermoScientific, USA) and Mycobacterium tuberculosis antibody PA1-7231 (Pierce Biotechnology, USA) was conducted.
Results of the study. The main sites of localization and clusters of MBT and their antigens were identified for various forms of lung MRT taking into account the degree of activity of a specific inflammatory process. The main antigen load is characteristic in the granulation layer of the cavern and capsule by the tubercle, as well as macrophage accumulations in the preserved alveoli outside the cavern or tuberculoma. Almost the same level of expression of MBT antigens is determined in the foci of specific tuberculous pneumonia at high degree of activity of the process. The established features of the distribution of MBT antigens in lung tissue cells in pulmonary tuberculosis suggest that it is the accumulations of macrophages in the alveoli at different distances from specific structures (caverns, tuberculomas) that are one of the most important anatomical and physiological factors for the further spread of specific inflammation in the lungs.
Expression of CD68 + cells, more pronounced in intensity and cell number, compared with infected macrophages, confirms the morpho-functional heterogeneity of macrophage cells during the development of tuberculosis lesions.
Key words: multidrug-resistant pulmonary tuberculosis, histological features, immunohistochemistry, macrophages.
Аннотация. В последние годы сохраняет актуальность изучение морфологических особенностей туберкулеза, вызванного резистентными штаммами МБТ. Влияние морфологически различной активности воспаления в момент оперативного лечения МРТБ легких с разными клиническими формами процесса на дальнейшее течение заболевания, результативность хирургического лечения остаются малоизученными. Уточнение морфологических характеристик туберкулезного процесса по операционному материалу имеет значение для прогноза дальнейшего развития процесса, уточнения характера местного иммунитета легких, что может служить базой для уточнения и выбора оптимальной дальнейшей тактики медицинского ведения этих больных.
Цель исследования: определение локализации и характера экспрессии клеток макрофагального ряда, в том числе – инфицированных микобактериями макрофагов в легочной ткани при разных формах мультирезистентного туберкулеза.
Материал и методы. Исследованы резецированные фрагменты легких 39 больных, с наличием туберкулемы, солитарной и множественных, или страдавших ФКТ легких. Во всех случаях при микробиологическом исследовании был установлен диагноз МРТБ легких. Среди пациентов было 19 мужчин (48,7 %) и 20 женщин (51,3 %), средний возраст был 32,7 ± 2,3 и 38,5 ± 9,7 лет соответственно. Выполнено традиционное гистологическое исследование пораженной легочной ткани, окрашенной гематоксилином и эозином, а также иммуногистохимическое исследование с использованием антител CD68 Clon КР1 (TermoScientific, США) и Mycobacterium tuberculosis antibody PA1-7231 (Pierce Biotechnology, США).
Результаты исследования: Были определены основные участки локализации и скоплений МБТ и их антигенов при разных формах МРТБ легких с учетом степени активности специфического воспалительного процесса. Основная антигенная нагрузка характерна для грануляционного слоя каверны и капсулы туберкулем, а также для скоплений макрофагов в сохранных альвеолах вне каверны или туберкулемы. Практически такой же уровень экспрессии антигенов МБТ определен в очагах специфической туберкулезной пневмонии при высокой степени активности процесса. Установленные особенности распределения антигенов МБТ в клетках легочной ткани при туберкулезе легких позволяют предположить, что именно скопления макрофагов в альвеолах на разной отдаленности от специфических структур (каверны, туберкулемы) являются одним из важнейших анатомо-физиологических факторов риска дальнейшего распространения специфического воспаления в легких.
Более выраженная по интенсивности и количеству клеток экспрессия CD68+ клеток в сравнении с инфицированными макрофагами, подтверждает морфо-функциональную гетерогенность клеток макрофагального ряда при развитии туберкулезного поражения.
Ключевые слова: мультирезистентный туберкулез легких, гистологические особенности, иммуногистохимия, макрофаги.
Постановка проблемы. Актуальность исследований, связанных с возникновением, развитием и медицинским ведением лекарственно-устойчивого туберкулеза, обусловлена постоянным ростом частоты случаев его встречаемости практически во всех регионах мира. Туберкулезный процесс, вызванный химиорезистентными микобактериями, особенно мультирезистентными штаммами или штаммами микобактерий туберкулеза (МБТ) с расширенной устойчивостью к химиопрепаратам, трудно поддается лечению, приводит к формированию тяжелых хронических, часто весьма распространенных, форм заболевания. До настоящего времени сохраняется низкая эффективность химиотерапевтического лечения мультирезистентного туберкулеза (МРТБ), несмотря на внедрение новых противотуберкулезных препаратов, совершенствование схем терапевтического лечения [11], что способствует длительному бактериовыделению у таких пациентов, формированию обширных деструктивных изменений, росту случаев как первичной, так и вторичной резистентности среди заболевших [6].
Хирургическое лечение туберкулеза является полезной стратегией в лечении МРТБ и туберкулеза с расширенной резистентностью согласно последним опубликованным результатам. Оно может быть составляющей при индивидуализированных режимах химиотерапии, причем успешный результат лечения превышает 90 % в случаях МРТБ, хотя при ТБ с расширенной резистентностью эффективность снижается [16].
Современный уровень торакальной хирургии, анестезиологии и интенсивной терапии позволяет расширить объем необходимой хирургической помощи разным группам больных туберкулезом органов дыхания. Эффективность хирургического лечения у впервые выявленных больных с ограниченными формами достигает 98%, а у больных с распространенным и прогрессирующим процессом, развившимися осложнениями она превышает 80%, хотя и снижается из-за позднего направления таких больных для хирургического лечения [12]. Хирургические методы были и остаются важным этапом в комплексном лечении больных туберкулезом органов дыхания и, в частности, с МРТБ легких.
Выделение нерешенных ранее частей общей проблемы. В последние годы возросло внимание к морфологическим особенностям туберкулеза, вызванного резистентными штаммами МБТ. Однако влияние активности воспаления (по морфологическим признакам), в частности, в предоперационный период и собственно на момент оперативного лечения МРТБ легких, на клинические формы процесса, длительность заболевания, результативность хирургического лечения остаются малоизученными [5].
Кроме того, в ряде случаев при гистологическом исследовании материала от больных с МРТБ возникают трудности диагностики заболевания и его активности, связанные со стертостью специфических признаков воспаления, отсутствием выраженной гранулематозной реакции в перифокальной области. В такой ситуации важное научно-практическое значение приобретает характеристика тканевых и клеточных реакций не только в очаге туберкулезного воспаления, но и окружающей легочной ткани [7]. Авторы подчеркивают важное диагностическое значение макрофагальной реакции в пораженной ткани, с учетом ее специфического характера [7].
Трудной задачей является определение активности процесса при такой форме легочного туберкулеза как туберкулема. Частое отсутствие клинико-рентгенологических и бактериологических признаков активности, таких как симптомы интоксикации, бактериовыделение, перифокальные инфильтративные изменения и распад, не исключает возможности морфологического выявления признаков высокой активности воспалительной реакции в казеозном очаге, его капсуле и в окружающих туберкулему тканях [15]. Подобный вывод сделан по результатам морфологического исследования резектатов легкого с туберкулезным поражением и другими исследователями [4]. Авторы подчеркивают значение определения степени активности туберкулезного воспаления при различных формах туберкулеза в предоперационном периоде, так как это имеет большое практическое значение в прогнозировании риска развития послеоперационных осложнений. Уточнение морфологических характеристик туберкулезного процесса по операционному материалу, в частности при фиброзно-кавернозном туберкулезе (ФКТ) легких, имеет значение для прогноза дальнейшего развития процесса, уточнения особенностей местного иммунитета легких у прооперированных пациентов, что может служить базой для уточнения и выбора оптимальной дальнейшей тактики медицинского ведения этих больных [2].
Важная роль в метаболизме легких, инициации и регуляции иммунного ответа на туберкулезную инфекцию принадлежит макрофагам, которые обладают значительным фагоцитарным и бактерицидным потенциалом, регулируют секреторную и пролиферативную активность других клеточных элементов, контролируют объем внеклеточного матрикса, инициируют и модулируют иммунные реакции. Соотношение числа активно фагоцитирующих и синтезирующих макрофагов не только отражает характер тканевой реакции, происходящей в зоне туберкулезного воспаления, но может служить показателем активности патологического процесса [14].
Цель данного исследования – определение локализации и характера экспрессии клеток макрофагального ряда, в том числе – инфицированных микобактериями макрофагов в легочной ткани при разных формах мультирезистентного туберкулеза.
Материалы и методы исследования. Материалом исследования служили резецированные фрагменты легких 39 прооперированных больных, с наличием туберкулемы, солитарной или множественных, или страдавших ФКТ легких. Во всех этих случаях при микробиологическом исследовании был установлен диагноз МРТБ легких. Среди пациентов было 19 мужчин (48,7 %) и 20 женщин (51,3 %), средний возраст пациентов составил 32,7 ± 2,3 и 38,5 ± 9,7 лет соответственно.
С момента выявления заболевания, до хирургического вмешательства, все пациенты получили основной курс специфической химиотерапии, с учетом профиля химиорезистентности штаммов МБТ в каждом случае. Длительность химиотерапии до операции составляла от 6 до 18 мес.
Для морфологического исследования туберкулем легких проводили вырезку фрагментов ткани легкого с наличием капсулы туберкулемы и частично – внутреннего некротического содержимого, а также близлежащей легочной паренхимы. В случаях ФКТ изучаемый фрагмент ткани легкого содержал участок стенки каверны и близко расположенные структуры легочной ткани.
Первым этапом гистологического исследования было уточнение степени активности специфического процесса по имеющимся морфологическим признакам при традиционном окрашивании гистологических срезов легких гематоксилином и эозином. Использовали ранее установленные и уточненные гистологические критерии активности туберкулезного воспаления [8, 9, 10]. По морфологическим признакам определяли высокую, умеренную и низкую степени активности специфического воспаления, которые соответствовали клиническому течению с прогрессированием, стабилизацией и регрессией туберкулезного процесса соответственно.
Серийные гистологические срезы пораженной туберкулезом ткани легких этих же пациентов были включены в иммуногистохимическое (ИГХ) исследование. Толщина срезов составляла 5-6 микрон. Использованы моноклональное антитело CD68 Clon КР1 (TermoScientific, США) и поликлональное кроличье Mycobacterium tuberculosis antibody PA1-7231 (Pierce Biotechnology, США).
Специфическое окрашивание проводили на AUTOSTAINER 360-2D, производства Thermo Fisher Scientific (США), использована система визуализации Ultra Vision Quanto HRP DAB (TermoScientific, США).
Учитывали локализацию клеток и вне клеточных структур с экспрессией антигенов к указанным антителам. Оценку интенсивности специфической реакции проводили полуколичественным методом, а именно было принято: + — слабое фоновое окрашивание, преимущественно желтого или темно-желтого цвета; ++ — окраска средней степени выраженности (средне-коричневый цвет) и +++ — выраженное темно-коричневое окрашивание клеток и/или жидких масс.
Микроскопическое исследование проводили на микроскопах Olympus CX21 и Olympus BX51 со встроенной фотокамерой Olympus DP73, микрофотографии получали, используя лицензионную программу cellSens Standard.
Полученные данные обработаны с использованием математических и статистических функций программы Microsoft Excel 2007.
Результаты исследования и их обсуждение. Выполнено традиционное морфологическое исследование гистологических препаратов легочной ткани с наличием хронической каверны или туберкулемы. Основными морфологическими признаками, которые учитывали при определении степени активности специфического воспаления при ФКТ, были характеристика стенки каверны и изменения легочной ткани в перикавитарной зоне. А именно, учитывали наличие и относительную толщину каждого из трех слоев хронической каверны; характер некротических изменений внутреннего слоя, клеточный состав грануляционного слоя, наличие гранулем разного клеточного состава в стенке каверны, выраженность фиброзного слоя. Вне каверны принимали во внимание наличие и выраженность неспецифических и специфических воспалительных изменений в соседних к каверне участках легкого, наличие и характер экссудативной реакции, гранулем с различным клеточным составом и выраженность некротических изменений внутри них; локализацию и численность лимфонодулей, характер развития и степень зрелости соединительной ткани [8, 9].
В случаях туберкулем легких обращали внимание на состояние внутренних казеозных масс (их уплотнение, кальцификацию или наоборот, их расплавление, со скоплением в них лейкоцитов), особенности развития капсулы туберкулемы – количество и степень выраженности ее слоев, в частности, развитие специфических грануляций и гранулем. В перифокальной зоне обязательно учитывали наличие или отсутствие пневмонических проявлений, экссудативной реакции, гранулем и их клеточный состав, степень зрелости и наличие фиброзных разрастаний, а также возможное наличие признаков специфического поражения бронхиальных структур [10].
Полученные результаты морфологической активности в каждом случае отражены в таблице 1.
Таблица 1
Количество случаев разных форм МРТБ легких с разной степенью
его активности по морфологическим признакам, абс.
| Форма-фаза туберкулеза легких | Высокая степень активности (прогрессирование ТБ) | Умеренно-низкая степень активности
(стабилизация или регрессия специфического воспаления) |
| Фиброзно-кавернозный туберкулез | 11 | 6 |
| Туберкулема легкого | 11 | 11 |
Частота встречаемости различных изменений легочной ткани при различных формах туберкулеза легких, с учетом активности специфического воспаления, представлена в таблицах 2 и 3.
Таблица 2
Морфологические признаки фиброзно-кавернозного туберкулеза легких
при разной активности специфического воспаления, количество наблюдений, абс. (%)
| Гистологическая структура | Высокая степень активности, n=11 | Умеренно-низкая степень активности, n=6 |
| Стенка хронической каверны: | ||
| – некротический слой | 10 (90,9) | 3 (50,0) |
| – грануляционный слой | 11 (100,0) | 6 (100,0) |
| – фиброзный слой | 11 (100,0) | 6 (100,0) |
| Гранулемы: | 9 (81,8) | 5 (83,3) |
| – в стенке каверны | 5 (45,5) | 4 (66,6) |
| – вне каверны | 8 (72,7) | 1 (16,6) |
| Экссудат в альвеолах | 9 (81,8) | 1 (16,6) |
| Макрофаги в альвеолах | 10 (90,9) | 6 (100,0) |
| Участки специфической пневмонии | 8 (72,7) | – |
При ФКТ легких с высокой активностью воспалительного процесса практически во всех наблюдениях в препаратах были представлены все три слоя хронической каверны, хотя их толщина значительно варьировала – как в одном и том же наблюдении, так и в разных случаях. Можно отметить, что чаще всего по толщине преобладал грануляционный слой, реже – некротический или фиброзный слои. Гранулемы выявлены в 9 (81,1 %) из 11 случаев при такой активности специфического воспаления. Они наблюдались как в стенке каверны, так и вне ее; в 4-х случаях гранулемы были представлены в обеих зонах исследования. По клеточному составу преобладали эпителиоидноклеточные гранулемы, причем в некоторых из них в центре выявлялся казеозный некроз. Также достаточно часто наблюдались гранулемы со значительным содержанием лимфоцитов и гигантских клеток Пирогова-Лангханса.
Вне структуры каверны в большинстве наблюдений (от 73 до 91 % случаев) в сохранных альвеолах определялись значительные скопления экссудата и/или клеток (преимущественно – макрофагов), а также признаки специфической пневмонии в виде липоидной пневмонии, инфильтратов из специфических грануляций с участками распада, скоплений туберкулезных гранулем. Фиброз легочной паренхимы – в виде различной толщины тяжей или очаговый, определялся во всех случаях – от умеренного до резко выраженного.
При умеренной (с тенденцией к снижению) активности воспалительного процесса во всех наблюдениях в препаратах были представлены грануляционный и фиброзный слои каверны, по толщине они были неравномерными, но чаще наиболее развитым был фиброзный слой. Некротический слой определялся в половине случаев, разной степени выраженности. Гранулемы наблюдали в большинстве случаев. Было замечено, что чаще всего они локализовались в стенке каверны, по морфологическим признакам они были «старыми», хотя и с некротическим центром. Экссудативная реакция практически исчезала. Значительные скопления клеток в альвеолах также не наблюдали, как правило, в одной альвеоле выявлялось 1-3 клетки. Специфических грануляций с морфологическими признаками активности вне каверны не было, обнаружены единичные «старые», инкапсулированные в фиброзную ткань, туберкулезные очаги.
Таблица 3
Морфологические признаки туберкулем легких
при разной активности специфического воспаления, количество наблюдений, абс. (%)
| Гистологическая структура | Высокая степень активности, n=11 | Умеренно-низкая степень активности, n=11 |
| Туберкулема: | ||
| – некротическое ядро | 11 (100,0) | 11 (100,0) |
| – грануляционный слой капсулы | 11 (100,0) | 8 (72,7) |
| – фиброзный слой капсулы | 9 (54,5) | 11 (100,0) |
| Гранулемы: | 8 (72,7) | 8 (72,7) |
| В капсуле туберкулемы | 6 (54,5) | 2 (18,2) |
| Вне туберкулемы | 8 (72,7) | 7 (63,6) |
| Экссудат в альвеолах | 6 (54,5) | 1 (9,1) |
| Макрофаги в альвеолах | 11 (100,0) | 6 (54,5) |
| Участки специфической пневмонии | 9 (81,8) | – |
Высокая степень активности в случаях туберкулем легких характеризовалась капсулой, в которой превалировал по выраженности грануляционный слой, хотя могли быть представлены как минимальные, так и выраженные разрастания фиброзного слоя. Последний отсутствовал только в случаях «молодой», только формирующейся туберкулемы. В некротических массах – ядре туберкулемы, как правило, обнаруживали очаги деструкции – краевой или в центральной области, где были представлены клеточный детрит и лейкоциты в разном количестве. В 6 (54,5 %) случаях в капсуле выявлены гранулемы различного клеточного состава, чаще всего – эпителиоидноклеточные с включениями единичных гигантских макрофагов (клеток Пирогова-Лангханса).
Вне структуры туберкулемы характерными признаками было наличие экссудативной реакции в соседних к туберкулеме альвеолах, 6 наблюдений (54,5%) (жидкость с большим содержанием фибрина, с включениями клеток макрофагального ряда). Как и в случаях ФКТ, важным диагностическим признаком было выявление участков специфической пневмонии, которые были выявлены в 9 (81,8 %) наблюдениях. Также диагностически значимым признаком было наличие специфического бронхиолита, при наличии бронхиол в срезах ткани (4 наблюдения, 36,4 %).
В отличие от ФКТ легких, при туберкулемах не наблюдали выраженного пневмофиброза.
При умеренно-низкой активности специфического воспаления определяли относительное уменьшение толщины грануляционного слоя капсулы туберкулемы, в ряде наблюдений (3 из 11), он вообще исчезал, тогда как всегда выявлялся фиброзный слой, который был различной толщины. В соседней с туберкулемой легочной ткани практически отсутствовала экссудативная реакция (только в одном наблюдении отмечен единичный участок альвеол с экссудатом), наблюдали относительное уменьшение гранулем – как в капсуле туберкулемы, так и вне нее. Причем, по гистологическому строению гранулемы относились к «зрелым» или имели признаки фибропластической трансформации. Участки специфической пневмонии не наблюдались, не выявляли признаков специфического бронхиолита.
Выполнен анализ локализации и полуколичественная оценка экспрессии CD68+ клеток и Ag MBT+ клеток (клеток с антигенами к МБТ) по серийным срезам этих же наблюдений. Известно, что антитело CD68 является неспецифическим маркером гистиоцитов и макрофагов различных типов, в том числе – их предшественников – моноцитов, а также гигантских многоядерных клеток. Возможна экспрессия CD68 фибробластами и эндотелиальными клетками [1, 19]. Важной особенностью этого маркера, несмотря на его неспецифичность, является высокая чувствительность к макрофагам, в частности, он демонстрирует отчетливую позитивную реакцию пенистых макрофагов, эпителиоидных клеток и клеток Пирогова-Лангханса при туберкулезном воспалении. Преобладает цитоплазматическая экспрессия, но возможна и умеренная мембранная.
Маркер антигенов МБТ выказывает как цитоплазматическую, так и мембранную экспрессию. Мы использовали поликлональное антитело к МБТ с учетом того, что оно обладает высокой чувствительностью к микобактериальной инфекции, но не является высокоспецифичным (положительно окрашивает микобактерии разных видов), а также вызывает фоновую окраску некоторых структур легочной ткани [3]. Специфичность исследования изначально была обеспечена микробиологической верификацией мультирезистентных штаммов МБТ.
Усредненный уровень интенсивности позитивной реакции клеток в разных участках легочной ткани при разных формах МРТБ легких представлен в таблицах 4 и 5.
Таблица 4
Характер и уровень экспрессии CD68+ клеток и AG MBT+ клеток
в различных структурах легочной ткани при ФКТ (МРТБ)
| Гистологическая структура | Фаза прогрессирования | Фаза стабилизации | ||
| Экспрессия Ag MBT | Экспрессия CD68+ | Экспрессия Ag MBT | Экспрессия CD68+ | |
| Стенка хронической каверны: | ||||
| – некротический слой | +/++ | ++ | +/– | +/– |
| – грануляционный слой | ++/+++ | +++ | ++/+++ | +++ |
| Гранулемы | +/+++ | +++ | +/++ | ++/+++ |
| Экссудат в альвеолах | +/+++ | –/++ | + | + |
| Макрофаги в альвеолах | +++ | +++ | +++ | +++ |
| Участки специфической пневмонии | ++ | +++ | – | – |
Примечание. Результаты по ряду гистологических структур представлены диапазоном интенсивности экспрессии вследствие выраженной гетерогенности уровня интенсивности в конкретной подгруппе.
Таблица 5
Характер и уровень экспрессии CD68+ клеток и AG MBT+ клеток
в различных структурах легочной ткани с туберкулемой (МРТБ)
| Гистологическая структура | Фаза прогрессирования | Фаза стабилизации/регрессии | ||
| Экспрессия Ag MBT | Экспрессия CD68+ | Экспрессия Ag MBT | Экспрессия CD68+ | |
| Туберкулема: | ||||
| – некротическое ядро | + | +/++ | + | + |
| – грануляционный слой капсулы | +/+++ | ++/+++ | +/++ | ++/+++ |
| Гранулемы | ++/+++ | ++/+++ | +/++ | ++/+++ |
| Экссудат в альвеолах | ++ | +/++ | + | + |
| Макрофаги в альвеолах | ++/+++ | +++ | +/+++ | ++/+++ |
| Участки специфической пневмонии | +/+++ | ++/+++ | – | – |
Примечание. Результаты по ряду гистологических структур представлены диапазоном интенсивности экспрессии вследствие выраженной гетерогенности уровня интенсивности в конкретной подгруппе.
Установлено, что характер и интенсивность экспрессии разных маркеров в клетках макрофагального ряда значительно варьировали, как в зависимости от изучаемой гистологической структуры, так и от уровня активности воспалительного процесса.
При ФКТ легких наиболее низкая экспрессия Ag MBT имела место в некротическом слое каверны, где не было сохранных клеток, а присутствовал клеточный детрит. Тем не менее, при высокой степени активности очагово отмечена позитивная – диффузно-гранулярная реакция среди масс некроза, тогда как в остаточных некротических массах при снижении активности процесса, как правило, отмечена только фоновая окраска. В этой же структуре положительная реакция к CD68 была более интенсивной, что можно объяснить скоплением в клеточном детрите разрушенных клеток-макрофагов (рис.1-2).
Максимальная интенсивность реакции обоих маркеров наблюдалась в клетках грануляционного слоя каверны, скоплениях макрофагов в альвеолах вне каверны и, несколько меньшая интенсивность реакции определена в клетках гранулем, независимо от расположения этих структур (табл. 4). Этот результат закономерен, поскольку именно в этих структурах имеются значительные скопления разных клеток макрофагального ряда.
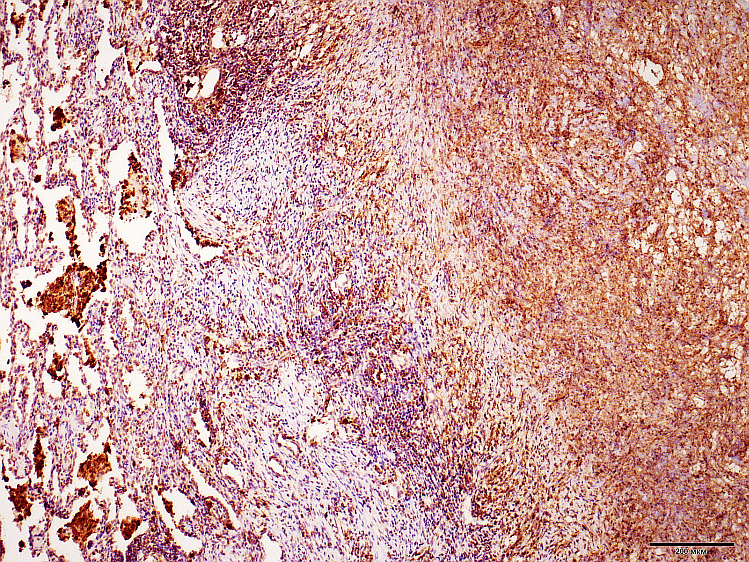
Рис. 1. На малом увеличении представлены стенка каверны (справа) с прилежащими альвеолами, в которых имеются скопления макрофагов. CD68+ клетки и клеточный детрит в стенке каверны, скопления макрофагов в альвеолах. Ув.: х 40.
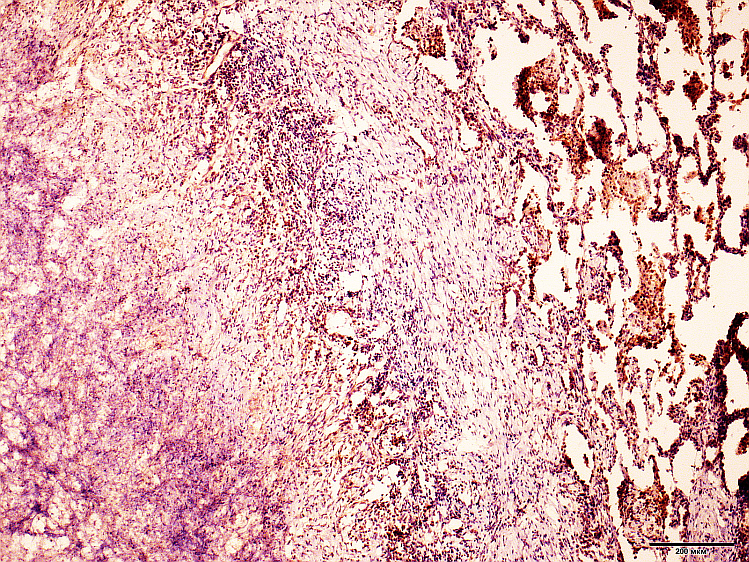
Рис. 2. То же наблюдение. Ag MBT-положительные клетки и клеточный детрит в стенке каверны (слева) и Ag MBT+-клетки в альвеолах. Ув.: х 40.
Также обращает внимание тот факт, что положительная экспрессия к Ag MBT практически во всех случаях определялась в относительно меньшем количестве макрофагальных клеток по сравнению с CD68+ клетками в этих же участках легочной ткани. Это подтверждает ранее установленный факт значительной морфо-функциональной гетерогенности макрофагов в развитии туберкулезного воспаления [13, 17, 18]. То есть, далеко не все клетки-макрофаги непосредственно принимают участие в фагоцитозе МБТ или их фрагментов, или иным образом контактируют с микобактериями.
Стоит отметить, что при наличии в перикавитарной зоне экссудативной реакции положительную реакцию окраски наблюдали только в случаях высокой активности специфического воспаления, причем максимальную интенсивность наблюдали только при маркере Ag MBT, что можно объяснить значительными скоплениями микобактериальных антигенов в альвеолярных пространствах.
Участки специфической туберкулезной пневмонии разных размеров и подтипов определялись только при высокой активности специфического воспаления, клетки макрофагального ряда демонстрировали отчетливую положительную реакцию на оба маркера (рис.3). Обращало внимание выраженное совпадение по локализации экспрессии обоих маркеров, что свидетельствовало о том, что практически все клетки-макрофаги содержали антигены МБТ в относительно разном количестве.
Рис. 3. МРТБ, ФКТ легких. Перикавитарная зона. А: CD68+ скопления клеток в гранулемах возле бронхиолы. Б: Ag MBT-положительные клетки в серийном срезе ткани этого же случая. Ув.: х100.
Несколько иной характер экспрессии установлен в случаях туберкулем легких, хотя основные характеристики (уровень экспрессии) во многом совпадали (табл. 4-5) по ряду гистологических образований, и с учетом степени активности специфического воспаления. Практически во всех наблюдениях некротическое ядро туберкулемы имело слабую (фоновую) экспрессию на оба маркера, не зависимо от степени активности воспалительного процесса. Уровень экспрессии и диапазон ее изменчивости в грануляционном слое капсулы туберкулемы, в имеющихся гранулемах практически совпадали по характеристике с грануляционным слоем каверны и гранулемами при ФКТ соответственно степени активности туберкулезного процесса. Этот же вывод можно сделать и в отношении экссудата в альвеолах, при обеих рассматриваемых формах туберкулеза легких, он практически исчезал при снижении активности воспаления (в обеих подгруппах было по 1 случаю), и имел фоновую реакцию окрашивания.
В отношении скоплений макрофагов в альвеолах, то при туберкулемах в разных наблюдениях отмечен более широкий диапазон позитивной реакции на антигены МБТ, в частности, при высокой степени активности. Вероятно, это связано с относительно меньшей антигенной нагрузкой макрофагов в случаях туберкулем чем при ФКТ легких. Подобные изменения наблюдались и в клетках макрофагального ряда в участках специфической пневмонии.
Выводы и перспективы дальнейших исследований. Таким образом, определены основные участки локализации и скоплений МБТ и их антигенов при разных формах МРТБ легких с учетом степени активности специфического воспалительного процесса. Основная антигенная нагрузка характерна для грануляционного слоя каверны и капсулы туберкулем, а также для скоплений макрофагов в сохранных альвеолах вне каверны или туберкулемы. Практически такой же уровень экспрессии антигенов МБТ наблюдается в очагах специфической туберкулезной пневмонии при высокой степени активности процесса. Кроме того, как показали наши исследования, уровни экспрессии антигенов МБТ весьма сходны в зонах значительного скопления клеток макрофагального ряда – в грануляционном слое каверны при ФКТ или капсулы туберкулем, и в гранулемах. Причем, антигенная нагрузка не зависит от локализации гранулем в легочной ткани, а в значительной степени определяется именно уровнем активности воспалительного процесса.
Установленные особенности распределения антигенов МБТ в клетках легочной ткани с различными формами туберкулеза легких позволяют предположить, что именно скопления макрофагов в альвеолах на разной отдаленности от специфических структур (каверны, туберкулемы) являются одним из важнейших анатомо-физиологических факторов возможности дальнейшего распространения специфического воспаления в легких.
Более выраженная по интенсивности и количеству клеток экспрессия CD68+ клеток как при ФКТ легких, так и в случаях туберкулем, в сравнении с инфицированными макрофагами, подтверждает морфо-функциональную гетерогенность клеток макрофагального ряда при развитии туберкулезного поражения.
Современные возможности иммуногистохимии позволяют проводить расширенные гистологические исследования МРТБ легких, с использованием целого набора различных ИГХ маркеров – как клеточных, так и энзимных, что позволит расширить наши познания тканевых клеточных взаимодействий и их приоритетность в патогенезе туберкулезного процесса. А учет химиорезистентности разных штаммов МБТ, возможно, поможет определить особенности конкретных клеточных реакций в связи с различными штаммами МБТ.
ЛИТЕРАТУРА
- Авербах М. М. Туберкулёзная гранулема. Современный взгляд на иммуногенез и клеточный состав // Туберкулёз и болезни легких. – 2010. – № 6. – С. 3–9.
- Ариэль Б.М., Елькин А.В., Басек Т.С., Осташко О.М., Кацер Л.И. Морфологические особенности фиброзно-кавернозного туберкулеза легких на операционном материале // Архив патологии. – 2004. – № 1. – С. 14–18.
- Гиляров А.В. Теоретические основы иммуногистохимического метода исследований – [Електронний ресурс]. – Режим доступу: http://www.labpoint.ru (labpoint.ru/upload/zagruzki/IGX_seminar.pdf).
- Елипашев А.А., Никольский В.О., Шпрыков А.С. Морфологические признаки активности воспаления при различных клинических формах лекарственно-устойчивого туберкулеза легких. Архив патологии. – 2017. – № 4. – С.13–17.
- Елипашев А.А., Никольский В.О., Шпрыков А.С. Прогностическое значение морфологических признаков активности туберкулезного воспаления у больных с ограниченными формами лекарственно-устойчивого туберкулеза легких // Архив патологии. – 2010. – № 4. – С. 40–43.
- Зюзя Ю.Р., Лепеха Л.Н., Гедымин Л.Е., Бурцева С.А. Ерохин В.В. Тканевые и клеточные реакции легких при лекарственно-устойчивом туберкулезе // Проблемы туберкулеза и болезней легких. – 2004.– № 8. – С.53–57.
- Зюзя Ю.Р., Лепеха Л.Н., Гедымин Л.Е., Бурцева С.А., Ерохин В.В. К вопросу о морфологической диагностике лекарственно-устойчивого туберкулеза легких // проблемы туберкулеза и болезней легких. – 2006. – № 10. – С. 56–60.
- Ліскіна І.В., Кузовкова C.Д., Загаба Л.М., Кравченко С.О., Вишневська Г.М. Морфологічна характеристика перикавітарної зони легень у випадках фіброзно-кавернозного туберкульозу з різним ступенем активності його перебігу // Український пульмонологічний журнал. – 2010. – № 4. – С. 12–14.
- Ліскіна І.В., Кузовкова С.Д., Загаба Л.М., Кравченко С.О., Лук’янчук В.Г. Морфологія стінки хронічної ригідної тришарової каверни у випадках фіброзно-кавернозного туберкульозу легень з різним ступенем активності його перебігу // Український пульмонологічний журнал. – 2010. – № 1. – С. 49–53.
- Ліскіна І.В., Кузовкова С.Д., Загаба Л.М., Лук’янчук В.Г. Сучасні гістологічні особливості туберкульом легень при різному ступені активності специфічного запального процесу // Сучасні інфекції. – 2010. – № 1. – С. 65–72.
- Мельник В.М., Новожилова І.О., Матусевич В.Г. Оцінка результатів лікування хворих на туберкульоз // Український пульмонологічний журнал. – 2018. – №4. – С. 35–41.
- Отс О.Н., Агкацев Т.В., Перельман М.И. Хирургические лечение туберкулеза легких при устойчивости микобактерий к химиопрепаратам. Проблемы туберкулеза и болезней легких.2009. – №2. – С. 42–49.
- Сахно Л.В., Черных Е.Р. Антигенпрезентирующие клетки при туберкулезе легких // Туберкулез и болезни легких. – 2012. – № 1. – С. 3–9.
- Филоненко Т.Г., Бисюк Ю.А. Функциональная активность макрофагов при фиброзно-кавернозном туберкулезе легких // Таврический медико-биологический вестник. – 2012, том 15, №2, ч.3 (58). – С. 252–257.
- Холодок О.А., Черемкин М.И. Морфологические аспекты активности туберкулом легкого // Амурский медицинский журнал. – 2014. – № 1 (5). – С. 40–43.
- Drug-resistant tuberculosis: past, present, future. Chiang C.-Y., Centis R., Migliori G.B. // Respirology. – 2010. – Vol.15. – P.413–432.
- Gordon S., Taylor P. R. Monocyte and macrophage heterogeneity // Nat. Rev. Immunol. – 2005. – Vol. 5. – P. 953–964.
- Guirado E., Schlesinger L. S., Kaplan G. Macrophages in Tuberculosis: friend or foe // Semin. Immunopathol. – 2013. – Vol.35 (5). – P. 563–583.
- Kunisch E. Macrophage specificity of three anti-CD68 monoclonal antibodies (KP1, EBM11, and PGM1) widely used for immunohistochemistry and flow cytometry / E. Kunisch, R. Fuhrmann, A. Roth [et al.] // Ann. Rheum. Dis. – 2004. – Vol. 63. – P. 774–784.